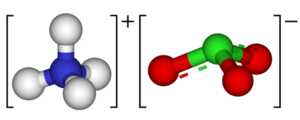Exploraremos en detalle la definición de clorato, sus propiedades, usos y ejemplos. Los cloratos son sales del ácido clórico (HClO3) que contienen cloro en estado de oxidación +V. Aunque son oxidantes fuertes, también pueden ser oxidados a percloratos (ClO4-). A continuación, examinaremos más de cerca estas sustancias y su importancia en diversas aplicaciones.
¿Qué es un clorato?
Un clorato es una sal que se forma a partir del ácido clórico (HClO3) y contiene cloro en estado de oxidación +V. Estas sales son compuestos químicos inorgánicos que se caracterizan por su alta inestabilidad y capacidad oxidante. No se encuentran en la naturaleza, pero se pueden sintetizar en laboratorio.
Propiedades de los cloratos
Los cloratos tienen varias propiedades distintivas que los hacen únicos:
- Son oxidantes fuertes: Los cloratos tienen la capacidad de ceder electrones y oxidar otras sustancias. Esta propiedad los hace útiles en diversas aplicaciones industriales y pirotécnicas.
- Inestabilidad: Los cloratos son compuestos altamente inestables y pueden descomponerse fácilmente bajo ciertas condiciones, liberando oxígeno y calor. Esta propiedad los hace peligrosos y requiere precauciones especiales al manipularlos.
- Reactividad con fósforo: Los cloratos reaccionan violentamente con el fósforo, lo que los convierte en una opción popular para encender cerillas y otros dispositivos de ignición.
Usos de los cloratos
Los cloratos tienen una variedad de aplicaciones en diferentes industrias:
Formulaciones pirotécnicas
Los cloratos se han utilizado tradicionalmente en formulaciones pirotécnicas debido a su capacidad oxidante y su capacidad para generar calor y luz. Sin embargo, debido a su inestabilidad y riesgo de explosión, se han ido reemplazando gradualmente por percloratos más seguros.
Elaboración de explosivos
Los cloratos también se han utilizado en la fabricación de explosivos debido a su alta capacidad oxidante. Sin embargo, debido a su inestabilidad y riesgo de explosión, su uso en esta área se ha reducido significativamente.
Fabricación de cerillas
Los cloratos se utilizan en la fabricación de cerillas debido a su reactividad con el fósforo. Cuando se raspa una cerilla en una superficie rugosa, el clorato reacciona con el fósforo, generando calor y encendiendo la cerilla.
Herbicidas
Los cloratos también se utilizan como herbicidas para controlar el crecimiento de malezas y plantas no deseadas. Su capacidad oxidante los hace efectivos para eliminar vegetación no deseada en áreas específicas.
Ejemplos de cloratos
Algunos ejemplos comunes de cloratos incluyen:
- Clorato de sodio (NaClO3)
- Clorato de potasio (KClO3)
- Clorato de amonio (NH4ClO3)
Conclusiones
Los cloratos son sales del ácido clórico que contienen cloro en estado de oxidación +V. Son oxidantes fuertes y se utilizan en diversas aplicaciones industriales, pirotécnicas y agrícolas. Sin embargo, debido a su alta inestabilidad y riesgo de explosión, su uso se ha reducido en algunos casos en favor de sustancias más seguras. Es importante manipular los cloratos con precaución y seguir las pautas de seguridad adecuadas al trabajar con ellos.