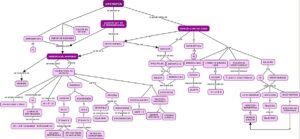
La entropía es una medida del desorden o la pérdida de orden en un sistema. Fue introducida por el físico Rudolf Clausius y se utiliza en diversas disciplinas como la física, la química, las matemáticas, la astrofísica, la lingüística, la computación y la ecología.
La entropía es un concepto fundamental en la termodinámica y se utiliza para describir el comportamiento de los sistemas físicos y químicos. También se aplica en otros campos, como la teoría de la información y la informática, donde se utiliza para medir la aleatoriedad y la falta de información en un sistema.
Definición de Entropía
La entropía se refiere al grado de irreversibilidad en un sistema termodinámico después de un proceso de transformación de energía. Es una medida del desorden o la falta de información en un sistema.
En la termodinámica, la entropía se define como la cantidad de energía que no puede ser utilizada para realizar trabajo. Se puede pensar en la entropía como una medida del número de formas en las que se puede distribuir la energía en un sistema.
La entropía se representa con la letra S y se mide en unidades de energía divididas por temperatura, como julios por kelvin (J/K).
Ejemplos de Entropía
Física
En física, la entropía se refiere al grado de irreversibilidad en un sistema termodinámico después de un proceso de transformación de energía. Por ejemplo, cuando se coloca un cubo de hielo en un vaso de agua a temperatura ambiente, el hielo se derrite y el agua se enfría hasta alcanzar el equilibrio térmico. Esto se debe a que el universo tiende a distribuir la energía de manera uniforme, aumentando así la entropía.
En este ejemplo, el hielo representa un estado de baja entropía, ya que las moléculas de agua están ordenadas en una estructura cristalina. Sin embargo, cuando el hielo se derrite, las moléculas de agua se dispersan y se distribuyen de manera más aleatoria, lo que aumenta la entropía del sistema.
Química
En química, la entropía se refiere a la medida de desorden en la formación de un compuesto químico. Por ejemplo, cuando se mezclan dos sustancias diferentes, la entropía aumenta debido a la mayor cantidad de posibles configuraciones moleculares.
Un ejemplo común es la mezcla de sal y agua. Cuando se disuelve sal en agua, las moléculas de sal se separan y se dispersan en el agua, lo que aumenta la entropía del sistema.
Astrofísica
En astrofísica, la entropía se observa en los agujeros negros, donde la cantidad de desorden es extremadamente alta debido a la concentración masiva de materia en un espacio muy pequeño.
Los agujeros negros son objetos extremadamente densos y compactos que tienen una gravedad tan fuerte que nada puede escapar de su atracción, ni siquiera la luz. Debido a esta alta concentración de masa en un espacio tan pequeño, la entropía en un agujero negro es extremadamente alta.
Teoría de la Información
En teoría de la información, la entropía se refiere al grado de incertidumbre en relación con un conjunto de datos. Cuanto mayor sea la entropía, mayor será la incertidumbre y la falta de información.
Por ejemplo, si se tiene un conjunto de datos en el que todos los elementos son iguales, la entropía será baja, ya que no hay incertidumbre ni falta de información. Sin embargo, si los datos son completamente aleatorios y no hay patrones discernibles, la entropía será alta.
Informática
En informática, la entropía se utiliza en criptografía para medir la aleatoriedad recogida por un sistema operativo o una aplicación. Cuanto mayor sea la entropía, más difícil será predecir los datos generados por el sistema.
La entropía se utiliza para generar claves de cifrado seguras y para garantizar que los datos generados por un sistema sean lo más aleatorios posible. Esto es especialmente importante en aplicaciones que requieren un alto nivel de seguridad, como las transacciones financieras en línea.
Neguentropía
La entropía también puede ser negativa, lo que se conoce como neguentropía. Esto ocurre en sistemas abiertos que pueden exportar entropía para mantener su propia entropía baja. Estos sistemas pueden compensar el proceso de degradación al que están sujetos a lo largo del tiempo.
Un ejemplo de neguentropía es el proceso de fotosíntesis en las plantas. Durante la fotosíntesis, las plantas utilizan la energía del sol para convertir el dióxido de carbono y el agua en glucosa y oxígeno. Este proceso reduce la entropía en el sistema de la planta, ya que se crea orden y se almacena energía en forma de glucosa.
Conclusión
La entropía es la medida del desorden en un sistema y se utiliza en diversas disciplinas para describir la irreversibilidad, el grado de incertidumbre y la aleatoriedad. Ejemplos de entropía se pueden encontrar en la termodinámica, la química, la astrofísica, la teoría de la información y la informática.